2024年2月14日,深圳大学高等研究院李猛教授团队在学术期刊《Cell Reports》发表了题为“Origin of eukaryotic-like Vps23 shapes an ancient functional interplay between ESCRT and ubiquitin system in Asgard archaea”的研究论文。该研究首次揭示阿斯加德古菌(Asgard archaea)内体分选转运复合体(ESCRT)核心功能亚基UEV-Vps23的起源模式,并阐明该亚基介导ESCRT和泛素修饰系统之间功能协作的分子机制。李猛教授为论文通讯作者,副研究员卢中一、博士生张思豫和刘杨教授为该论文的共同第一作者,深圳大学为唯一单位。
内膜系统的出现是细胞内物质运输方式由原核生物细胞的简单自由扩散向真核生物细胞的主动分选转运演化的分水岭,是解答真核生物起源这一生命科学领域重大基础科学问题的关键线索之一。特别是,真核生物内膜系统物质分选功能的实现,需要ESCRT识别及分选被泛素化修饰的货物蛋白;因此,揭示ESCRT和泛素化修饰系统之间功能协作机制建立及演化过程,是探究真核生物内膜系统起源的重要前提。
李猛教授研究团队以阿斯加德古菌ESCRT核心功能亚基UEV-Vps23为研究切入点(图1),发现该亚基的蛋白结构域包括UEV和Vps23 domain;其中UEV介导该亚基识别古菌泛素分子,Vps23 domain可被古菌泛素修饰系统标记修饰,并且UEV和Vps23 domain通过相互作用使该亚基呈现的自抑制状态,可能是调节阿斯加德古菌ESCRT和泛素修饰系统之间功能协作的重要分子基础。此外,研究团队首次提出阿斯加德古菌UEV-Vps23可能起源于基因融合,该亚基是古菌CdvA向真核生物Vps23演化的“过渡版本”,进而为阿斯加德古菌向真核生物演化过程中新基因起源模式提供科学依据。
该研究得到国家自然科学基金(32225003、32393970、32393971、92251306、32370004)、广东省基础与应用基础研究基金(2023A1515011309)、深圳大学2035计划(2022B002)等项目资助。论文链接:https://doi.org/10.1016/j.celrep.2024.113781。
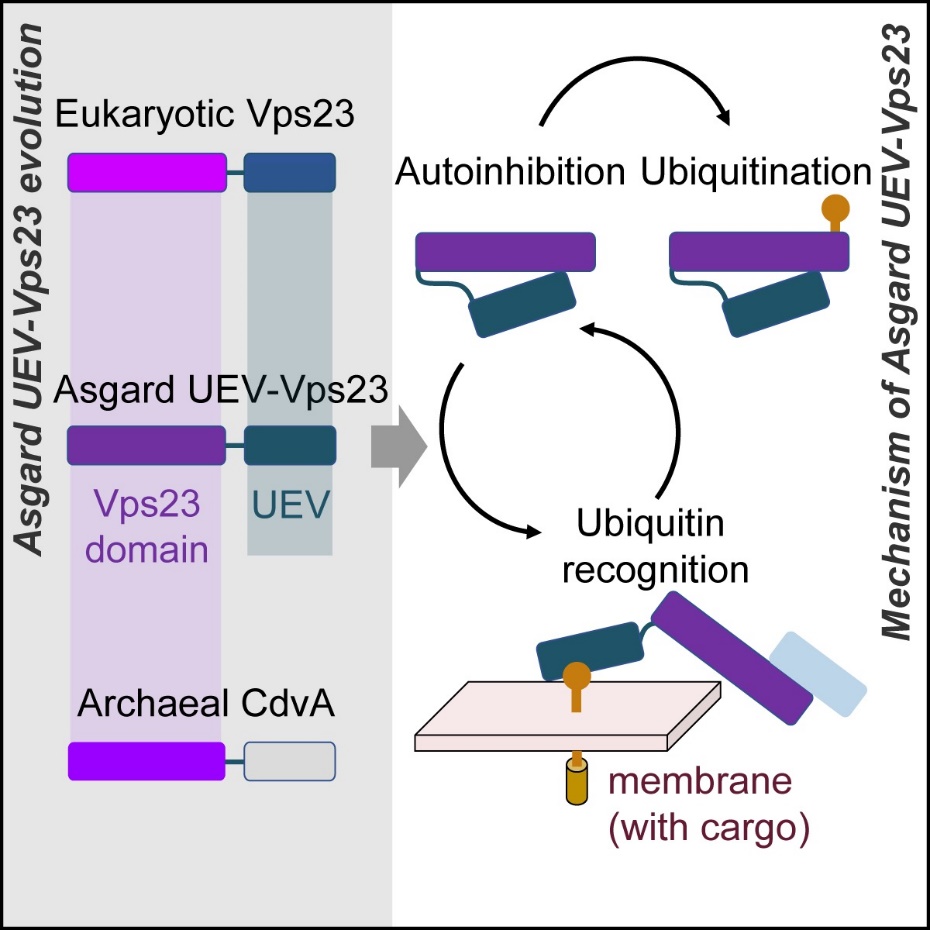
图1阿斯加德古菌UEV-Vps23功能演化机制


