教育背景:
2004.09—2009.07,中国科学院化学研究所,化学,博士
2000.09—2004.07,清华大学,化学系,学士
工作经历:
2022.07—至今, 深圳大学,高等研究院,研究员、副教授
2016.07—2022.06, 深圳大学,高等研究院,研究员、助理教授
2016.01—2016.06, 中国科学院化学研究所,副研究员
2015.01—2016.05, 美国纽约州立大学石溪分校,化学系,访问学者
2009.07—2016.01, 中国科学院化学研究所,助理研究员
2019.02—现在, 美国马里兰大学,材料科学工程,兼职副教授
学术兼职:
美国物理学会,会员
所获奖项:
2016年深圳市海外高层次人才计划:孔雀计划C类
2017年中国·南京新材料创客大赛三等奖
2018年深圳市南山区领航人才
2018年挑战杯·创青春广东大学生创业大赛铜奖指导老师
2021年优秀本科教师奖
2021年深圳大学2021届百篇优秀本科毕业论文指导教师
2021年研究生新锐导师
2023年优秀本科教师奖
研究兴趣:
一、高性能植入型医疗器械的设计开发及性能评价
1.高分子材料在神经修复领域的应用
严重的神经外周损伤需要通过手术修复治疗。临床上对于5mm以下的小缺损一般直接以缝线吻合。而接近或大于10 mm的长距离神经缺损则需要缝入植入物进行桥接。以往通常以自体或异体神经组织作为修复的植入物,但这两类植入物来源有限,且易造成供区损伤或排斥反应。
本研究以静电纺丝技术为基础,开发出的可吸收合成高分子材料促神经修复导管为基础,重点研究导管的表界面结构及生物力学性能的精确调控对重构外周神经局部微环境的影响,阐明其在组织细胞水平和蛋白基因水平促进神经修复的生物学机制,并将优化结构转化应用于临床研究,为外周神经缺损提供全合成材料物理调控的解决方案,也为组织修复的微环境重构重要性提供科学理论依据。

2.多层级控释系统的设计开发、控释机理及应用尝试研究
根据最新的《2020年癌症统计》,全球癌症的发病率和死亡率依然在迅速增长。癌症是威胁人类身体健康最危险的疾病之一,开展针对这种重大疾病的治疗方法、药物和制剂的研究,实现癌症的有效治疗,是关系到人民生活质量的重要科学课题。由于开发一个新的药物需要很长的研发周期和巨额的研究费用,因此采用新的载药体系则是一个快速可行的有效方法。
本研究所提出的多级药物控释体系,主要针对恶性肿瘤手术治疗后的多种副反应,通过深入探究生物降解材料对机体不同生理周期的顺应性机理,利用静电纺丝技术,实现其体系理化性能的精确调控,探索材料界面-细胞的相互作用行为与机制,实现肿瘤诱导生长转移和可控原位给药治疗的协同调控策略治疗模式,从而解决提升患者生存质量的关键问题。

3.植入高分子材料在软组织修复的应用、与生物基体相互作用研究
细胞外微环境信号可在细胞-细胞外基质(ECM)界面调控细胞行为和功能,其促进软组织修复与再生的作用日益受到关注。
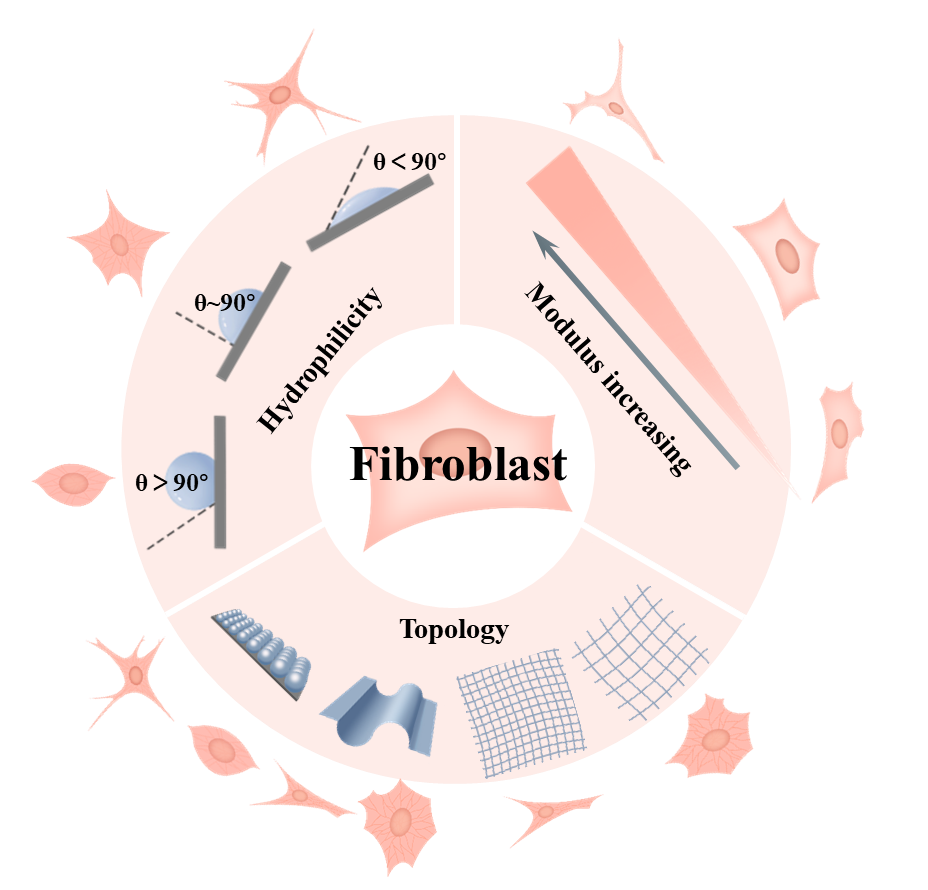
本研究利用植入高分子材料构建组织工程支架,模拟ECM提供微环境线索,从而影响细胞形态、迁移、增殖和分化。微观生物力学作为动态的微环境线索,对维持细胞骨架和ECM之间的力学平衡至关重要。重点关注目前微环境线索的构建策略,旨在阐明细胞-细胞外基质界面微观生物力学线索在调节细胞行为中的作用。最终对开发新一代软组织修复生物材料提出了新的关注点和研究思路。
二、相结构、晶型与材料性能研究
1.聚稀烃共混物在动力学对称及非对称下的分相、结晶及形貌、性能控制
作为当今21世纪使用最多的塑料材料,聚烯烃在加工过程中能够形成特殊的分相形态和结构,并由此获得了特殊的性能,也成为了凝聚态理论的热门研究体系。本研究选用HDPE/CFC-11等共混体系,研究其在动力学对称及非对称下的分相、结晶及形貌、性能的控制。
2.高温高压下聚合物相分离动力学、结晶动力学及形貌学研究
闪蒸纺丝是通过将聚合物溶液溶解于特殊的纺丝溶剂,在高压情况下喷出来制备极细纺丝的方法。共混溶液在高温高压情况下达到均相状态,最终通过喷头喷出,压力快速降低,纺丝溶剂迅速蒸发,聚合物长链结晶并因为超音速流被快速拉伸成极细纤维。闪蒸纺丝一般有着极强的机械性能,和很好的防水透气性,多用于防护服和医用服装产业。本课题致力于借助闪蒸纺丝控制喷出时的均相状态来控制最终产出纤维的形态和性能,研究高温高压状态下聚合物相分离和结晶的动力学。
科研项目:
国家级和省市级项目
1.国家自然科学基金委面上项目,基质刚性的精确调控指导治疗肿瘤的侵袭和转移,2021-01至2024-12,58万元,国家自然科学基金委,在研,主持。
2.深圳市科技创新委员会基础研究面上项目,微纳塑料经口毒性研究及食品污染防控标准的建立,2021-10至2024-10,60万,在研,主持。
3.深圳市高端人才科研启动项目,植入器械的设计开发及临床前评价,2018-01至2020-12,300万元,已结项,主持。
4.深圳市知识创新计划基础研究项目,靶向载药纤维膜用于肿瘤术后化疗,2017-08至2020-03,49万元,已结项,主持。
5.国家自然科学基金青年基金项目,超细纤维膜的防粘连和抗感染功能化研究,2012-01至2013-12,25万元,已结题,主持。
横向项目
1.深圳市光远生物材料有限责任公司,用于肿瘤术后放疗的载药纤维膜的测试分析及材料评估,2019-06至2021-06,20万元,主持。
2.北京天助畅运医疗技术股份有限公司,用于长期植入生物稳定性材料的分析及评估,2019-01至2019-12,10万元,主持。
3.宁波光远致信生物科技有限公司,诱导型组织修复材料,2020-10至2021-09,50万元,主持。
4.北京天助畅运医疗技术股份有限公司,植入材料及器械的临床前评价,2021-01至2021-12,100万元,主持.
研究队伍
研究助理:王洁,余江凌,韦锐月
博士后:孙承媚
硕士研究生:黄诗芬,陈灏,李圣美,王骝,徐嘉蔚,王慧锦

培养学生获奖:
1. 2018年广东省大学生创新创业训练计划项目结题学生:伍家恩、陈灏
2. 2018年挑战杯.创情春广东大学生创业大赛铜奖学生:王岚
3. 2018年深圳大学学生创新发展基金基础实验项目三等奖学生:伍家恩
4. 2018年深圳大学“挑战杯”大学生课外学术科技作品竞赛结项学生:伍家恩
5. 2019年深圳大学荣誉学位学生:伍家恩
6. 2019年深圳大学第二届高研院本科毕业论文论坛奖学生:伍家恩
7. 2019年深圳大学本科生学生论坛二等奖学生:周伟贤
8. 2019年深圳大学“荔园挑战”创新创业大赛三等奖学生:陈灏
9. 2020年深圳大学荣誉学位学生:黄诗芬
10. 2020年深圳大学第三届高研院本科毕业论文论坛奖学生:黄诗芬
11. 2020年深圳大学优秀硕士生源选拔合格学生:陈灏
12. 2020年深圳大学学生创新发展基金基础实验项目优秀学生:陈灏
13. 2021年深圳大学百篇优秀本科毕业论文学生:陈灏
14. 2021年深圳大学年度“荔园之星”学生:陈灏
15. 2021年硕士研究生国家奖学金学生:伍家恩
16. 2022年“建行杯”第八届中国国际“互联网+”大学生创新创业大赛学生:陈梓博、甄毅
17.深圳大学第十一届“我们面试吧”大赛暨首届“荔园选才会”技术赛道特等奖学生:甄毅
18. 2022年深圳大学“荔园挑战”创新创业大赛铜奖学生:李圣美、陈灏、王骝、徐嘉蔚
19. 2022年深圳大学年度“荔园之星”学生:陈灏
20. 2023年深圳大学第九届中国国际“互联网+”大学生创新创业大赛校赛研究生创意组第二学生:陈灏
21. 2023年深圳大学第九届中国国际“互联网+”大学生创新创业大赛校赛本科生创意组第一学生:甄毅
22. 2023年深圳大学第九届中国国际“互联网+”大学生创新创业大赛校赛本科生创意组第二学生:陈梓博
已毕业学生情况:
李涵,工作,深圳小学科学教师,食品安全与毒理学;
刘子凡,硕士在读,佛罗里达大学,磁性材料;
周伟贤,博士在读,中国科学院纳米中心,纳米材料;
张瑜健,博士在读,威斯康星大学麦迪逊分校,化学教育;
伍家恩,博士在读,普林斯顿大学,化学与生物工程;
陈旭鸿,博士在读,麻省大学阿默斯特分校,高分子科学与工程;
明天昊,博士在读,麻省大学罗威尔分校,高分子化学。
学术论文:
1.Hao Chen, Jiaen Wu, Muhammad Saif Ur Rahman, Shengmei Li, Jie Wang, Shilin Li, Yan Wu, Ying Liu*,Shanshan Xu*, Dual drug-loaded PLGA fibrous scaffolds for effective treatment of breast cancer in situ,Biomaterials Advances(2023),148,213358.
2.Zhenyu Lin, Hao Chen, Jiawei Xu, Jie Wang, Huijing Wang, Shifen Huang,Shanshan Xu*, A Review of the Release Profiles and Efficacies of Chemotherapy Drug-Loaded Electrospun Membranes, Polymers (2023), 15, 251.
3.Hao Chen, Muhammad Saif Ur Rahman, Shifen Huang, Shengmei Li, Jie Wang, Kexin Li, Yan Wu, Ying Liu*,Shanshan Xu*, Sandwich-like scaffold for effective hemostasis and anti-adhesion in cardiac injury, Materials & Design (2023), 225, 111533.
4.Muhammad Saif Ur Rahman, Jiaen Wu, Hao Chen, Chengmei Sun, Ying Liu,Shanshan Xu*, Matrix mechanophysical factor: pore size governs the cell behavior in cancer, Advances in Physics: X (2023), 8 (1), 2153624.
5. Zhipeng Zeng, Yajing Yang, Junyong Deng, Muhammad Saif Ur Rahman, Chengmei Sun*,Shanshan Xu*, Physical Stimulation Combined with Biomaterials Promotes Peripheral Nerve Injury Repair, Bioengineering (2022), 9, 292.
6.Shanshan Xu, Chenhong Wang, Ruoqing Mao, Xiaoyu Liang, Heran Wang, Zhenyu Lin, Jiangxue Li, Shilin Li, Jipeng Jiang, Tongshuo Zhang, Yongfu Ma, Yang Liu, Charles C. Han, Ying Liu*, Surface structure change properties: Auto-soft bionic fibrous membrane inreducing postoperative adhesion, Bioactive Materials (2022), 12: 16-29.
7. Nuozi Zhang, Chenhong Wang, Hao Chen, Jiaen Wu, Charles C. Han andShanshan Xu*, Electrospun fibrous membrane with confined chain configuration: dynamic relaxation and glass transition, Polymers, (2022), 14(5):939.
8. Shifen Huang#, Yiming Zhang#, Chenhong Wang*, Qinghua Xia, Muhammad Saif Ur Rahman, Hao Chen, Charles Han, Ying Liu* andShanshan Xu*, Mechanisms affecting physical aging and swelling by blending an amphiphilic component, International Journal of Molecular Sciences (2022), 23:2185.
9. Chenhong Wang#, Zifan Liu#, Nuozi Zhang#, Shifen Huang, Ruoqing Mao, Heran Wang, Qinghua Xia, Charles C. Han,Shanshan Xu*, Ying Liu*; Three dimensional fibrous scaffolds as tissue repairing templates during post-operative healing, Materials & Design (2021), 210:110019.
10. Luoan Shen, Qinyi Gan, Youcheng Yang, Cesar Reis, Zheng Zhang,Shanshan Xu, Tongyu Zhang and Chengmei Sun*, Mitophagy in Cerebral Ischemia and Ischemia/Reperfusion Injury, Frontiers in aging neuroscience (2021), 13:687246.
11. Shilin Li#,Shanshan Xu#, Xiaoyu Liang, Yueguang Xue, Jie Mei, Yongfu Ma, Yang Liu, and Ying Liu*, Nanotechnology: breaking the current treatment limits of lung cancer, Advanced Healthcare Materials (2021), 10:2100078.
12. Jiaen Wu,Shanshan Xu*, Charles C. H and Guangcui Yuan*, Controlled drug release: on the evolution of physically entrapped drug inside the electrospun poly (lactic-co-glycolic acid) matrix, Journal of Controlled Release (2021), 331:472-479.
13. Hao Chen, Xuhong Chen, Huiying Chen, Xin Liu, Junxing Li, Jun Luo, Aihua He, Charles C. Han, Ying Liu,Shanshan Xu*; Molecular interaction, chain conformation, and rheological modification during the electrospinning of hyaluronic acid aqueous solution, Membranes (2020), 10:217.
14. Zixin Zhang#, Kexin Li#, Weixian Zhou#, Jin'ge Gu, Ying Liu, Charles C. Han andShanshan Xu*; Factors influencing the interactions in Gelatin/Hydroxyapatite hybrid materials, Frontiers in Chemistry (2020), 8:489.
15. Jiaen Wu#, Zixin Zhang#, Jin’ge Gu#, Weixian Zhou, Xiaoyu Liang, Guoqiang Zhou, Charles C. Han,Shanshan Xu*, Ying Liu*; Mechanism of a long-term controlled drug release system based on simple blended electrospun fibers, Journal of Controlled Release (2020), 320: 337-346.
16. Qinghua Xia#, Nuozi Zhang#, Jiangxue Li#, Heran Wang, Chenhong Wang, Zixin Zhang, Jin’ge Gu, Mengjie Wang, Charles C. Han,Shanshan Xu*, Ying Liu*; Dual-functional esophageal stent coating composed of paclitaxel-loaded electrospun membrane and protective film, Journal of Biomedical Nanotechnology (2019), 15(10): 2108-2120.
17. Xinxing Zhu, Yawei Yan, Chunzhi Ai, Shan Jiang,Shanshan Xu, Min Niu, Xiangzhen Wang, Genshen Zhong, Xifeng Lu, Yu Xue, Shaoqi Tian, Guangyao Li, Shaojun Tang, Yizhou Jiang*, Jarid2 is essential for the maintenance of tumor initiating cells in bladder cancer, Oncotarget (2017), 8(15):24483-24490.
18. Xinxing Zhu, Yawei Yan, Demeng Chen, Chunzhi Ai, Xifeng Lu,Shanshan Xu, Shan Jiang, Genshen Zhong, Dongbao Chen, Yizhou Jiang*, Long Non-coding RNA HoxA-AS3 interacts with EZH2 to Regulate Lineage Commitment of Mesenchymal Stem Cells,Oncotarget(2016), 7(39):63561-63570.
19. Zixin Zhang, Jianxiong Tang, Heran Wang, Qinghua Xia,Shanshan Xu*, Charles Han*. Controlled antibiotics release system through simple blended electrospun fibers for sustained antibacterial effects. ACS Applied Materials & Interfaces (2015), 7, 26400−26404.
20. Qinghua Xia, Ziwen Liu, Chenhong Wang, Zixin Zhang,Shanshan Xu*, and Charles C. Han* A biodegradable trilayered barrier membrane composed of sponge and electrospun layers: hemostasis and antiadhesion. Biomacromolecules (2015), 16, 3083-3092.
21. Chenhong Wang, Kuo Zhang, Heran Wang,Shanshan Xu*, Charles C. Han*, Evaluation of biodegradability of poly (DL-lactic -co-glycolic acid) scaffolds for post-surgical adhesion prevention: in vitro, in rats and in pigs. Polymer (2015), 61, 174-182.
22. Ming Cheng, Heran Wang, Zhen Zhang, Nan Li, Xiaohong Fang*,Shanshan Xu*, Gold nanorod-embedded electrospun fibrous membrane as a photothermal therapy platform. ACS Applied Materials & Interfaces (2014), 6 (3), 1569–1575.
23. Heran Wang, Ming Cheng, Jianming Hu, Chenhong Wang,Shanshan Xu* and Charles C Han*. Preparation and optimization of silver nanoparticles embedded electrospun membrane for implant associated infections prevention. ACS Applied Materials & Interfaces (2013), 5 (21), 11014–11021.
24. Heran Wang, Min Li, Jianming Hu, Chenhong Wang,Shanshan Xu*, Charles C. Han*. Multiple targeted drugs carrying biodegradable membrane barrier: anti-adhesion, hemostasis and anti-infection. Biomacromolecules (2013) 14: 954-961.
25. HuarongNie, Junxing Li, Aihua He*,Shanshan Xu, Qingsong Jiang, Charles C Han*, Carrier system of chemical drugs and isotope from gelatin electrospun nanofibrous membranes, Biomacromolecules (2010), 11(8):2190-2194.
26. HuarongNie, Aihua He*, jianfenzheng,Shanshan Xu, Charles C Han*, Effect of poly(ethylene oxide) with different molecular weights on the electrospinnability of sodium alginate, Polymer (2009), 50(20):4296-4934.
27.Shanshan Xu, Junxing Li, Aihua He*, Wenwen Liu, Xingyu Jiang, Jianfen Zheng, Charles C. Han*, Dufei Fang, Benjamin S. Hsiao, Benjamin Chu. Chemical crosslinking and biophysical properties of the electrospun hyaluronic acid based ultra-thin fibrous membranes. Polymer (2009) 50: 3762-3769.
28.Shanshan Xu, Jun Zhang, Aihua He*, Junxing Li, Hao Zhang, Charles C. Han*. Electrospinning of native cellulose from nonvolatile solvent system, Polymer (2008) 49: 2911–2917.
29. Huarong Nie, Aihua He*, Jianfen Zheng,Shanshan Xu, Junxing Li, Charles C. Han*, Effects of chain conformation and entanglement on the electrospinning of pure alginate, Biomacromolecules (2008), 9(5):1362-1365.
30. Hua Wang, Changmei Cheng*, Hongchao Zheng, Xiaohong Liu, Chang Fang,Shanshan Xu, Yufen Zhao, Study on disulfur-backboned nucleic acid: part 2, efficient synthesis of 3 ,5 -dithiothymidine, Chemistry Letters (2005),34(3):432-433.
31. Hongchao Zheng, Changmei Chen*, Hua Wang,Shanshan Xu, Yufen Zhao, Study on disulfur-backboned nucleic acid: part 1, efficient synthesis of 3',5'-dithio-2'-deoxyadenosine, Synlett(2004),14:2585-2587.
专利情况
累计申请国家专利140余项,已获授权专利62项,授权专利中已有24个进入产业化阶段,以下仅列举部分:
1.韩志超、许杉杉、伍家恩,一种载药纳米纤维膜及其制备方法和应用,2021-12-14,中国,CN201910197875.8.
2.陈灏、伍家恩、许杉杉、刘颖、韩志超,一种病灶原位药物控制释放系统及其制备方法,2022-01-07,中国,CN201911205722.X.
3.韩志超、许杉杉、伍家恩、王岚,一种载药纳米复合纤维膜系统及其制备方法和应用,2022-05-03,中国,CN201910198279.1.
4.韩志超;许杉杉;诱导生长型可吸收补片的制备方法, 2016-12-21,中国, CN201210444940.0.
5.韩志超;许杉杉;一种用于抗癌药物传输的响应型纳米纤维的制备方法, 2015-6-3,中国, CN201310586339.X.
6.韩志超;许杉杉;佴刚;一种用于软组织再生的纳米纤维的制备方法, 2015-7-15,中国, CN201310586082.8.
7.韩志超;许杉杉;一种自粘止血防粘连纤维体的制备方法, 2015-2-18,中国, CN201310594072.9.
8.张瑜健;许杉杉;徐海阳;一种可调节药物释放行为的载药纤维膜及其制备方法,2018-11-19,中国, 201811377100 .0.
8.韩志超;许杉杉;一种酸性环境中可实现药物快速释放的智能型多功能空心微球及其制备方法, 2012-2-22,中国, CN201110347250.9.
10.韩志超;许杉杉;一种使用抗菌组合物制备缓释抗菌膜和植入材料的方法, 2016-2-10,中国, CN201310594218.X.
学术报告及会议:
2017年11月,国际高分子与凝聚态物理特别讨论会,深圳,主办
2018年03月,The APS March Meeting,美国洛杉矶,邀请报告:Physical or Chemical Aging of PLGA Electrospun Fibers Related to its Sequence Distribution
2023年4月,高分子科学前沿讲座,中国北京,报告题目:植入医疗器械的产学研之路


